| PDF-FD療法は歯周病治療の補助療法として有望ですが、現時点では標準治療ではありません。 組織修復を促す可能性が示唆されていますが、臨床試験は限定的です。 本治療は自由診療であり、症状や疾患によっては適応外のケースがあります。 効果は個人差があり保証できません。 学術論文は、必ずしも治療効果を保証するものではありません。 本記事は一般的な医学情報の提供を目的としています。 治療の適応については医師にご相談ください。 |
| 執筆:ナールス美容医療アカデミー編集長 富本充昭 |
<はじめに>
歯周組織再生療法は近年大きく進歩し、歯周病治療の考え方そのものが変化しつつあります。
本記事は、歯周病治療の選択肢を検討している患者様や、再生療法に関心のある方に向けて解説するものです。
歯周病は日本人が歯を失う主な原因とされ、進行すると歯槽骨や歯根膜などの歯周組織が不可逆的に破壊される慢性疾患です。
近年の歯周治療では炎症の抑制にとどまらず、失われた歯周組織の回復を目指す治療の重要性が高まっています。
こうした歯周組織再生療法の進展を背景に、自己血由来の成長因子を活用する治療は「成長因子療法」として注目されています。バイオロジック製剤に分類されるPDF-FD(Plasma Derived Factors – Freeze Dried)療法もその一つであり、PRP療法の概念を応用した細胞非含有(Cell Free)製剤を用いることで、品質の安定性や再現性の向上が期待されています。
組織修復環境の改善を目的とし、特に垂直性骨欠損(intrabony defect)を伴う症例では補助的治療として検討されることがあります。
ただし、これらの治療は決して万能ではなく、すべての症例に適応できるわけではありません。
PDF-FD療法は有望な補助療法の一つですが、現時点では歯周病治療の標準治療として確立されているわけではないことも理解しておく必要があります。
治療効果は骨欠損の形態や炎症の程度、全身状態など多くの要因に影響されるため、現在のエビデンスを正しく理解し、基本治療を基盤としたうえで症例に応じた適切な治療選択を行うことが重要です。
本記事では、「歯周病に本当に効果があるのか」「安全性は十分に検証されているのか」「GTR法やエムドゲインとどう違うのか」といった疑問に答えるため、PDF-FD療法の作用メカニズム、臨床エビデンス、適応条件、リスクについて医学論文に基づき客観的に解説します。
歯周病とは?失われる歯周組織と治療の課題
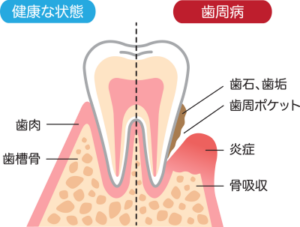
歯周病は、歯を支える組織に慢性的な炎症が生じることで進行する疾患であり、日本人が歯を失う主な原因とされています【1】【2】。
初期段階では自覚症状が少ないものの、進行すると歯槽骨や歯根膜が破壊され、最終的には歯の動揺や脱落につながる可能性があります。
近年では、単なる口腔内の疾患にとどまらず、全身の健康にも影響を及ぼす慢性炎症性疾患として注目されています。
1)歯周病の原因と進行プロセス
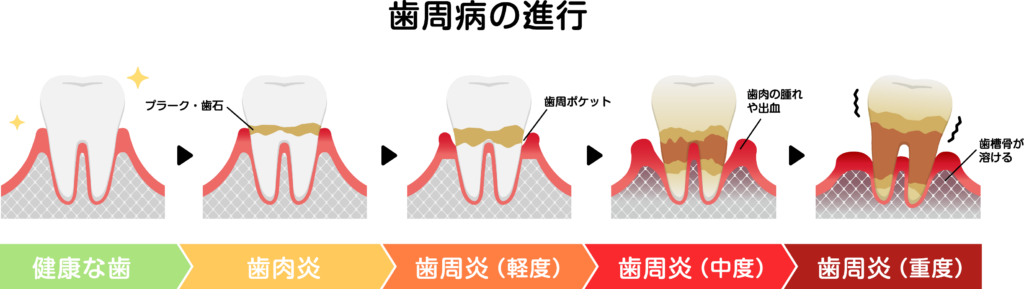
歯周病の主な原因は、歯の表面に付着する細菌性プラーク(歯垢)です。プラーク内の細菌が毒素を産生すると歯肉に炎症が起こり、腫れや出血といった症状が現れます。」この段階は「歯肉炎」と呼ばれ、適切な口腔ケアによって改善が期待できます。
しかし炎症が長期化すると、歯と歯肉の間に「歯周ポケット」が形成され、内部で嫌気性菌が増殖しやすい環境が生まれます。やがて炎症は歯肉だけでなく、歯槽骨や歯根膜といった支持組織へと波及し、骨吸収が進行します。
この状態が歯周炎であり、自然に元の状態へ戻ることは難しいとされています【4】。
特に問題となるのは、歯槽骨が一度失われると完全に回復することが容易ではない点です。そのため、歯周病治療では炎症のコントロールに加えて、失われた組織をいかに修復・再生させるかが重要な課題となります。
2)歯槽骨・歯根膜・歯肉の役割と破壊の影響
歯は単独で存在しているわけではなく、複数の歯周組織によって支えられています。
- 歯槽骨:歯を顎骨に固定する土台
- 歯根膜:咬合時の衝撃を吸収するクッション
- 歯肉:細菌の侵入を防ぐバリア
これらの組織が健全に保たれることで、歯は長期的に機能します。
しかし歯周病が進行すると、これらの支持構造が段階的に破壊され、歯の安定性が低下します。歯根膜の損傷は咬合時の負担増加を招き、さらに骨吸収を加速させる可能性があります。
また、歯肉が退縮すると知覚過敏や審美的な問題を引き起こすこともあります。
このような支持組織の破壊は不可逆的となる場合が多く、従来の治療だけでは完全な回復が難しいことが、歯周病治療における大きな課題とされています。
3)歯周病が全身に及ぼす影響
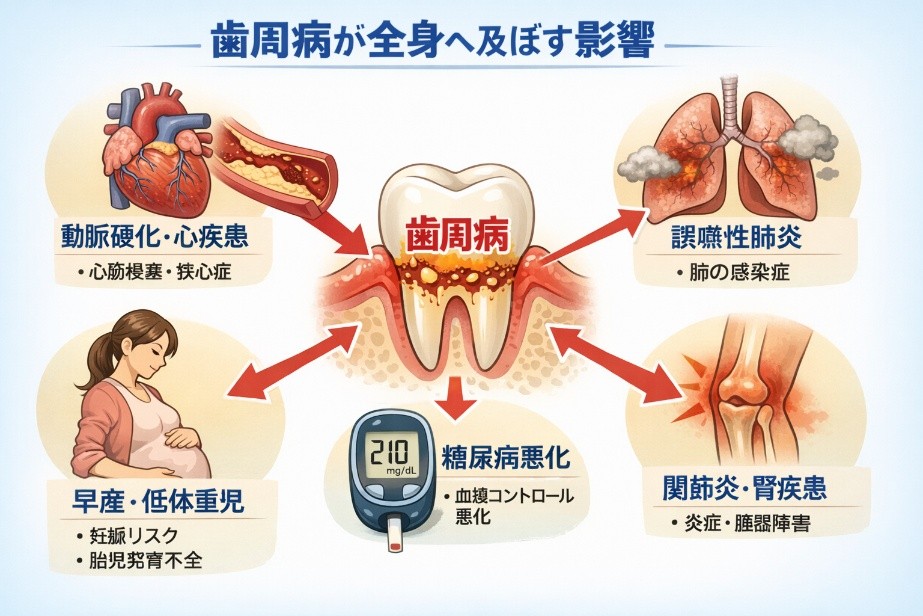
近年の研究では、歯周病が全身の健康と密接に関連している可能性が指摘されています。
また、重度歯周炎は世界で6番目に多い疾患とされており、公衆衛生上も重要な課題とされています【3】。
歯周組織で生じた慢性炎症は炎症性サイトカインの産生を促し、血流を介して全身へ影響を及ぼすと考えられています。
特に、糖尿病とは双方向の関係があるとされ、血糖コントロールの不良は歯周病の重症化を招き、逆に歯周病の炎症がインスリン抵抗性を高める可能性があります。また、因果関係が解明されてはいませんが、動脈硬化や心血管疾患との関連を支持する研究も報告されています。【5】。
このような背景から、歯周病は単なる歯科疾患ではなく、全身の健康管理の一環として捉える必要があります。
4)従来の歯周病治療の限界

歯周病治療の基本は、原因となる細菌の除去です。スケーリングやルートプレーニングによって歯石や感染組織を取り除くことで、炎症の改善が期待できます。
しかし、これらの基本治療はあくまで病状の進行を抑えることを目的としており、失われた歯周組織そのものを再生する治療ではありません。
重度の骨欠損を伴う症例では、歯の保存が困難になるケースもあります。
こうした課題を背景に、「破壊された組織の再生を目指す治療」への関心が高まり、歯周組織再生療法が注目されるようになりました。近年では、成長因子を活用して組織の修復環境を整える再生医療適なアプローチも研究されています。
その1つがPRP療法や今回紹介するPDF-FD療法です。
本記事では、PubMed等に掲載された医学論文および臨床研究をもとにPRP療法やPDF-FD療法の効果や安全性を紹介します。
歯周組織再生療法という考え方

歯周病治療はこれまで、炎症の原因となる細菌を除去し、病状の進行を抑えることが主な目的とされてきました。
しかし近年では、「失われた歯周組織の回復を目指す」という概念が重視されるようになり、歯周組織再生療法が注目されています。
歯周組織再生療法とは、歯槽骨・歯根膜・セメント質といった歯を支える構造の再建を目的とする治療アプローチです。単なる修復ではなく、本来の組織に近い状態での機能回復を目指す点に特徴があります。すべての症例で完全な再生が得られるわけではありませんが、適切な症例を選択することで歯の長期保存につながる可能性があります。
1)再生療法が目指す治療とは
組織の「修復」と「再生」は似ているようで異なる概念です。修復は損傷部位を瘢痕組織などで補う過程を指すのに対し、再生は元の構造や機能に近い状態を取り戻すことを意味します。歯周治療において再生が重要視されるのは、支持組織の機能が回復することで歯の予後が改善する可能性があるためです。
再生療法の成功には、いくつかの生物学的条件が必要とされています。
代表的な考え方として知られるのが「組織再生の三要素」です【6】。
- 細胞(Cells):新たな組織を形成する主体
- 足場(Scaffold):細胞が増殖するための構造
- シグナル分子(Growth Factors):細胞の分化や増殖を促す因子
近年は、このうち成長因子を活用して組織修復環境を整える治療戦略が関心を集めています。
2)代表的な歯周組織再生療法
現在の歯科臨床では、いくつかの再生療法が症例に応じて使い分けられています。
以下の3つは代表的な再生医療です。
①GTR法(歯周組織誘導法)
GTR(Guided Tissue Regeneration)は、バリアメンブレンと呼ばれる特殊な膜を用いて歯肉の侵入を防ぎ、歯根膜や骨の再生を促す治療法です。特に骨内欠損に対して適用されることが多く、長年にわたり臨床実績が蓄積されています【7】。
歯周ポケット内の汚れをきれいに除去した後、人工骨を詰め、その上からメンブレンで覆い、歯周組織の再生を待つという治療です。
GTR法は、広い範囲の再生を促すことができるため、ほかの治療法では難しい状態でも治療ができる点がメリットです。
また、保険適用となるため費用の負担が軽減される点もメリットです。
②エムドゲイン(エナメルマトリックスタンパク)
エムドゲインは、歯の発生過程に関与する特殊なタンパク質を応用し、歯周組織の再生を促すことを目的とした生物学的製剤です。垂直性骨欠損などで良好な結果が報告されており、現在も広く使用されています【8】。
歯根部分のクリーニングを行った後、歯槽骨が溶けてしまった部分にエムドゲインを塗布し再生を促す方法です。
エムドゲイン法は、外科手術が一回で済むため、患者さんの負担が少ない点がメリットです。しかし、保険適用にはなっておらず経済的な負担が大きくなる点がデメリットです。
③リグロス(トラフェルミン使用法)
リグロス(トラフェルミン使用法)は、細胞成長因子を利用した歯周組織再生療法です。
トラフェルミンは細胞の活性化を促す作用があり、患部に塗布することで歯肉や骨の再生を助けます【9】。
歯根部分のクリーニングを行った後にトラフェルミンを塗り込み、再生を促す治療法です。
リグロスは、外科手術が一回で済むため、患者さんの負担が少ない点がメリットです。
また、リグロスは保険適用となるため患者さんの経済的負担も小さく済みます。
一方、適応できるケースが限られることや効果を実感できるまでの期間が長い点がデメリットです。
3)新たな再生医療的アプローチ
今、紹介した3つの代表的な歯周病の再生医療に加えて新たなアプローチが登場しています。
①自己血液由来製剤による治療(PRP療法やPDF-FD療法)
自己血から抽出した血小板には、多数の成長因子が含まれています。これらを局所に適用することで、創傷治癒の促進や骨再生の補助が期待されています。外科治療や骨補填材と併用されるケースも多く、補助的治療としての位置づけが確立しつつあります。
近年では、こうした血小板由来製剤の概念を基盤としながら、成長因子をより安定的に活用することを目的とした新しいアプローチも登場しています。その一つが、血漿由来因子を凍結乾燥して製剤化したPDF-FD療法です。
PDF-FD療法は細胞を含まない成長因子製剤であり、再生医療等安全性確保法に基づく「再生医療」には該当しませんが、組織修復環境を整える再生誘導型の治療として研究が進められています。
②幹細胞培養上清液の注射
幹細胞培養上清液とは、幹細胞を培養する過程で分泌される成長因子やサイトカインなどの生理活性物質を豊富に含んだ液体成分のことです。幹細胞そのものは含まれていませんが、組織修復や再生を促す多様な因子が含まれているため、歯周組織の治療への応用が研究されています【6】。
培養上清液に含まれる成長因子には、血管新生を促進する因子や抗炎症作用を持つ因子、細胞の増殖・分化を促す因子などが含まれており、これらが複合的に作用することで組織修復環境の改善が期待されます。
治療としては、歯周外科処置の際に患部へ注入する、あるいは歯周ポケット内に注射するといった方法が検討されています。幹細胞そのものを移植するわけではないため、倫理的・技術的なハードルが比較的低く、また取り扱いも容易である点が特徴です。
ただし、現時点では研究段階にある治療法であり、標準的な歯周治療として確立されているわけではありません。製剤の品質管理や投与方法、適応症例の選定など、臨床応用に向けた課題も残されています。
③幹細胞による再生医療
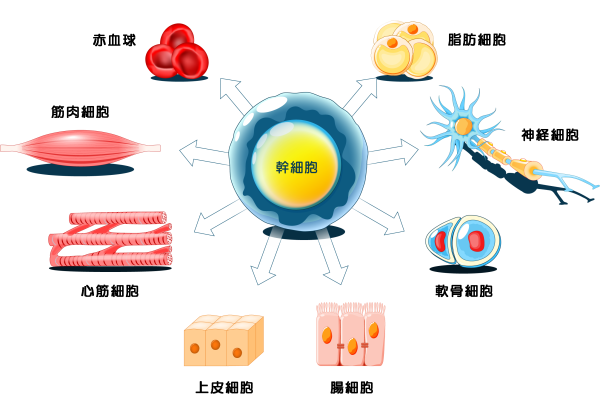
幹細胞を用いた歯周組織再生は、再生医療の中でも最も先進的なアプローチの一つです【6】【10】。
幹細胞は自己複製能力と多分化能を持つ細胞であり、適切な条件下で歯槽骨・歯根膜・セメント質などの歯周組織へと分化することが可能とされています。
歯周領域で注目されている幹細胞には、骨髄由来間葉系幹細胞、脂肪組織由来幹細胞、歯髄幹細胞、歯根膜幹細胞などがあります。
これらの幹細胞を患者自身の組織から採取・培養し、欠損部位に移植することで、失われた歯周組織の再生を促すという治療戦略です。
実験的研究では、幹細胞移植により骨や歯根膜様組織の形成が確認されており、将来的な臨床応用への期待が高まっています。
特に、患者自身の細胞を使用する自家移植であれば、拒絶反応のリスクが低い点もメリットとして挙げられます。
一方で、幹細胞治療は再生医療等安全性確保法の規制対象となるため、実施には厳格な安全性・有効性の確認が必要です。また、細胞の採取・培養には高度な技術と設備が必要であり、コストも高額になる傾向があります。現状では研究段階の治療法であり、保険適用もされていないため、一般的な歯科診療として受けられる段階には至っていません。
今後、技術の進歩や臨床研究の蓄積により、より安全で効果的な幹細胞治療が確立されれば、歯周病治療の選択肢として大きな可能性を持つと考えられています。
<参考記事>
PDF-FD(C-PRP)療法とは何か

PDF-FD療法は、自己血由来の成長因子を活用して組織修復環境を整えることを目的とした治療アプローチです。PDF-FDは Plasma Derived Factors – Freeze Dried(血漿由来因子の凍結乾燥) の略称であり、血液中に含まれる成長因子を抽出・濃縮したうえで凍結乾燥し、製剤化したものを指します。
従来のPRP血小板由来製剤と同様に創傷治癒過程へ関与する生理活性物質を利用しますが、保存性や品質の安定化を重視した設計が特徴とされています【11】。なお、細胞成分を含まないため、再生医療等安全性確保法に基づく「再生医療」には該当しません。あくまで成長因子の働きを通じて組織の修復環境を整える再生誘導型アプローチとして位置づけられます。
1)PDF-FD療法の定義と正式名称
PDF-FD療法とは、患者自身の血液から得られる血漿中の成長因子を活用する治療法です。成長因子は本来、創傷治癒の過程で重要な役割を担っており、細胞の増殖や分化、血管新生などを調整するシグナル分子として機能します【11】。
これらの因子を局所に適用することで、歯周組織の修復を促しやすい環境を整えることが期待されています。ただし、失われた組織を直接再生させる治療ではなく、生体が本来持つ治癒能力を補助するアプローチである点を理解しておくことが重要です。
2)Cell Free(細胞非含有)の意味と重要性
PDF-FD製剤は細胞を含まない、いわゆるCell Free製剤です。これは幹細胞治療などの細胞移植型再生医療とは異なる点であり、制度上の再生医療に該当しない理由の一つでもあります。
細胞を含まないことにより、細胞の生存率や品質ばらつきといった要因の影響を受けにくく、比較的均一な製剤設計が可能になると考えられています【11】。
また、免疫反応のリスクが理論的に低い点も特徴とされています。
ただし、自己血由来であっても医療行為である以上、感染予防や適切な製剤管理が不可欠です。凍結乾燥PRPを用いた臨床研究においても安全性が評価されており、臨床応用に向けた基盤が整いつつあります【12】。
3)凍結乾燥技術による安定性と再現性
PDF-FD療法の大きな特徴の一つが、成長因子を凍結乾燥(フリーズドライ)する工程です。凍結乾燥により水分が除去されることで、成長因子の活性を保持しながら長期保存が可能になるとされています【13】。
従来のPRPでは採血後比較的短時間で使用する必要がありましたが、凍結乾燥製剤では保存性が向上するため、治療計画の柔軟性が高まる可能性があります【11】。
また、製剤の品質を一定に保ちやすい点も臨床上の利点として考えられています。
さらに、凍結乾燥後であってもPDGF受容体を介したシグナル伝達の活性化など、生物学的機能が維持される可能性が報告されています【14】。
もっとも、成長因子の活性維持や最適な投与条件については、今後さらなる研究が求められています。今後さらなる研究が求められています。
4)PRP療法との違い
PDF-FD療法は、自己血由来の成長因子を活用するという点でPRP療法と共通していますが、製剤設計にはいくつかの違いがあります。
①保存性
PRPは採血後に速やかに使用する必要がありますが、PDF-FDは凍結乾燥により保存性の向上が期待されています【11】【13】。
②品質の均一性
PRPは調製方法によって血小板濃度が変動する可能性があります。一方、PDF-FDは製剤化の過程を経ることで、より安定した品質を目指した設計とされています【11】。
③投与タイミング
保存可能な製剤であることから、外科処置のタイミングに合わせた使用が検討しやすい点も特徴です【11】。
さらに、凍結乾燥PRPは新鮮PRPと比較しても成長因子の保持や機能が維持され得ることが報告されています【15】。
<PRP療法とPDF-FD療法の違い
| PRP療法 | PDF-FD療法 | |
| 保存性 | 長期保存が困難 | 凍結乾燥により長期保存が可能 |
| 成分安定性 | 時間経過や温度変化の影響を受けやすい | 成長因子の活性を比較的安定した状態で保持 |
| 再現性 | 採血条件や調製方法によるばらつきが生じやすい | 工程管理により品質の均一化が図られる |
ただし、現時点ではPDF-FDがPRPより臨床的に優れていると結論づける十分なエビデンスはなく、両者の位置づけについては今後の研究動向を踏まえて判断する必要があります。
<参考記事>
PDF-FD(C-PRP)療法とは?効果・安全性・適応疾患をエビデンスで検証
歯周病における主な成長因子の作用
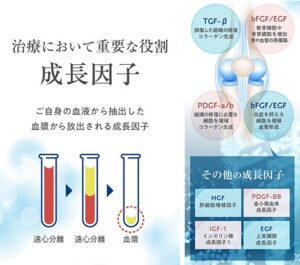
歯周組織の修復には、多様な成長因子が相互に関与しています。
これらは本来、創傷治癒の過程で分泌され、細胞の増殖・分化、血管形成、細胞外基質の生成などを調整するシグナル分子として機能します。
PDF-FD療法では、こうした成長因子を局所に供給することで、歯周組織の修復が進みやすい環境を整えることが期待されています。ただし、成長因子のみで組織が再生するわけではなく、基本治療による炎症コントロールが前提となります。
1) PDGF(血小板由来成長因子)
PDGFは創傷治癒の初期段階で重要な役割を担う因子です。線維芽細胞や骨芽細胞の遊走を促し、損傷部位へ修復細胞を集める働きがあるとされています。さらに細胞増殖を刺激することで、歯根膜や歯槽骨の修復過程を支える可能性があります。
2)TGF-β(トランスフォーミング増殖因子β)
TGF-βはコラーゲン産生を調整し、細胞外基質の形成を促進すると考えられています。これにより組織の構造的安定性が高まり、創傷部位の強度向上に寄与する可能性があります。また炎症反応の調整にも関与するとされています。
3)VEGF(血管内皮増殖因子)
VEGFは新たな血管の形成を誘導する代表的な因子です。血流が改善されることで、酸素や栄養素が修復部位に供給されやすくなり、治癒環境の向上につながると考えられています。
4)FGF(線維芽細胞増殖因子)
FGFは線維芽細胞の増殖を促し、肉芽組織の形成に関与します。さらに血管新生を補助する作用も報告されており、軟組織の修復を支える因子の一つとされています。
5)IGF(インスリン様成長因子)
IGFは細胞の分化やタンパク質合成を促進し、骨形成に関与する可能性が示唆されています。骨芽細胞の活性化を通じて、歯槽骨の修復環境を整える役割が期待されています。
6)EGF(上皮成長因子)
EGFは上皮細胞の増殖を促進し、創傷部位の被覆を早める働きがあるとされています。歯肉組織の回復を支えることで、感染リスクの低減にも寄与する可能性があります。
重要なのは、これらの成長因子が単独で作用するのではなく、相互に影響し合いながら創傷治癒を進める点です。
例えば、
- PDGF → 修復細胞を呼び寄せる
- VEGF → 血流を改善する
- TGF-β → 組織を安定させる
といった流れが連続的に起こることで、修復環境が整うと考えられています。
しかし、成長因子はあくまで生体が本来持つ治癒能力を支援するものであり、単独で失われた歯周組織を完全に再生させるものではありません。
治療効果は骨欠損の形態や炎症の程度、全身状態など多くの要因に影響を受ける可能性があります。
| 成長因子 | 主な作用 | 歯周組織への期待される働き |
| PDGF | 細胞遊走・増殖 | 歯根膜・骨修復の支援 |
| VEGF | 血管新生 | 栄養供給の改善 |
| TGF-β | コラーゲン形成 | 組織安定化 |
| FGF | 線維芽細胞増殖 | 軟組織修復 |
| IGF | 骨芽細胞活性化 | 骨形成支援 |
| EGF | 上皮増殖 | 歯肉回復 |
歯周病に対するPDF-FD療法のエビデンス

本章では、主にシステマティックレビューやランダム化比較試験など、エビデンスレベルの高い研究を中心に、歯周病に対する血小板由来製剤およびPDF-FD療法の有効性を整理します。
1)歯周組織再生療法としての位置づけ
PDF-FD(C-PRP)療法は、歯周病治療における歯周組織再生療法の一選択肢として研究が進められている治療アプローチです【16】。歯周病が進行すると、歯槽骨・歯根膜・歯肉といった支持組織が破壊され、従来の基本治療(スケーリングやルートプレーニング)のみでは失われた組織の回復が困難となる場合があります。
こうした背景から、血小板由来成長因子を活用した再生誘導治療が注目されています。PDF-FD療法はPRP療法の概念を基盤としながら、成長因子を凍結乾燥することで保存性や品質の安定化を図った製剤を用いる点に特徴があります。
なお、細胞成分を含まないため再生医療等安全性確保法上の「再生医療」には該当しませんが、成長因子の作用を通じて歯周組織の修復環境を整える補助的治療として期待されています。
2)血小板由来製剤を用いた歯周治療のアンブレラレビュー
血小板由来製剤を用いた歯周組織再生療法については、複数のシステマティックレビューやメタ解析を統合したアンブレラレビューが報告されています【16】。
Ardilaらによる2023年のアンブレラレビューでは、PRF、L-PRF、PRPといった血小板由来製剤の臨床効果が評価されました。その結果、歯周ポケット内骨欠損に対する治療において、PRFは外科治療単独と比較して臨床的アタッチメントレベル(CAL)の有意な獲得をもたらすことが示されています【17】【18】。
さらに、歯周ポケット深さ(PD)の減少においても統計的に有意な改善が認められ、放射線学的骨充填に関しても外科治療単独より優れた結果が報告されています【17】【19】。
ただし、これらの研究の多くはPRFやPRPを対象としており、PDF-FD単独の高品質エビデンスは現時点では限定的である点には留意が必要です【16】。
3)改善を示唆する研究と限界を示す研究
血小板由来製剤の効果については改善を示唆する研究が蓄積されている一方、その有効性には症例条件や治療方法による差があることも報告されています。
骨補填材と併用した研究では、歯周ポケット深さの減少、臨床的アタッチメントレベルの獲得、放射線学的骨再生の促進が認められる傾向があります【19】【20】。特に、垂直性骨欠損を伴う中等度歯周炎では補助療法として有用である可能性が示されています【20】。
一方、重度歯周炎や広範な骨欠損を伴う症例では、血小板由来製剤単独で十分な再生効果を得ることは難しいとされています。また、治療効果は術式、欠損形態、患者の全身状態などの影響を受ける可能性があります【16】。
このように、血小板由来製剤は万能な治療ではなく、適切な症例選択が重要です。
4)歯周外科治療との併用における効果
PDF-FD療法は単独で用いられるよりも、歯周外科治療と併用することで効果が高まる可能性があると考えられています。
フラップ手術では歯肉を切開して歯根面や骨欠損部を直接処置できるため、PDF-FD製剤を局所に適用することで成長因子が線維芽細胞の活性化、血管新生、炎症制御に関与すると推測されています。
さらに、自家骨や人工骨などの骨補填材と併用することで、物理的な足場(scaffold)と生物学的刺激の双方を提供できる可能性があります。このような併用療法は、単独治療と比較して臨床的アタッチメントレベルの獲得や骨充填率の向上に寄与する傾向が報告されています【21】。
5)エビデンスレベルの評価と現時点での結論
①エビデンスの質
- 血小板由来製剤全般に関するランダム化比較試験(RCT)は複数存在する【20】。
- システマティックレビューやメタ解析も蓄積されつつある【16】【17】。
- ただし、PDF-FDに特化した大規模RCTは現時点で限定的である【16】。
②効果の評価
- 軽度〜中等度歯周病における補助的治療として臨床的有用性が示唆される【17】【19】。
- 外科治療単独と比較してPD減少やCAL獲得に寄与する可能性がある【17】。ただし、失われた組織を完全に再生する治療ではない。
③現時点での結論
PDF-FD療法は、歯周病治療における補助的な選択肢として期待される治療アプローチですが、現段階では確立された標準治療とは位置づけられていません。基本治療や適切なメンテナンスを前提としたうえで、症例に応じて慎重に適用することが重要です。
また、製剤の品質管理、投与量、治療プロトコルの標準化など、今後さらなる臨床研究の蓄積が求められます。
PDF-FD療法の適応となる歯周病と向かないケース
PDF-FD療法は成長因子を活用して組織修復環境を整える補助的治療であり、すべての歯周病症例に適応されるわけではありません。
治療効果は歯周病の進行度や骨欠損の形態、患者の全身状態などに影響を受ける可能性があるため、適切な症例選択が重要とされています。
また、基本治療によって炎症がコントロールされていることが前提条件となる場合が多く、再生療法のみで歯周病の改善を目指すものではない点を理解しておく必要があります。
1)適応が推奨されるケース
①軽度〜中等度の歯周病
歯周ポケットが比較的浅く、歯槽骨の残存量が一定程度保たれている症例では、生体の治癒能力が働きやすく、補助療法の効果が得られる可能性があります。
②垂直性骨欠損を伴う症例
骨が垂直方向に吸収しているケースでは、再生療法の適応となることがあります。骨欠損部に成長因子を適用することで、修復環境の改善が期待されます。
③歯周外科治療後の組織修復を促したい場合
フラップ手術などの外科処置と併用することで、創傷治癒を補助する目的で使用が検討されることがあります。
④歯の保存を優先したいケース
抜歯を回避し、可能な限り天然歯を維持したい場合に、包括的治療の一環として選択されることがあります。
2)適応外となる可能性があるケース
①重度の骨吸収を伴う歯周病
歯槽骨の喪失が著しく、歯の支持がほとんど残っていない場合には、再生療法のみで十分な改善が期待できないことがあります。
②急性炎症が持続している状態
強い腫脹や排膿が認められる場合は、まず感染のコントロールが優先されます。炎症が安定していない状態では再生環境が整いにくいとされています。
③口腔衛生状態が不良な場合
プラークコントロールが不十分だと炎症が再燃しやすく、治療結果に悪影響を及ぼす可能性があります。
3)慎重な判断が求められるケース
①喫煙習慣がある場合
喫煙は血流を低下させ、創傷治癒を遅延させる要因となることが知られています。そのため、再生療法の効果にも影響を及ぼす可能性があります。
②糖尿病などの全身疾患がある場合
血糖コントロールが不良な状態では感染リスクや治癒遅延が生じやすく、治療計画を慎重に検討する必要があります。
③免疫機能が低下している場合
全身状態によっては、外科処置を伴う治療の適応を慎重に判断することが望ましいとされています。
4)症例選択が治療結果を左右する
再生療法や類似のアプローチの成否は、治療法だけで決まるものではありません。欠損形態、歯の動揺度、咬合状態、患者の生活習慣など、多くの要因が治療結果に影響すると考えられています。
そのため、PDF-FD療法は単独で効果を期待する治療ではなく、基本治療、外科治療、メンテナンスを含めた包括的な歯周治療の中で検討されることが重要です。歯科医師による適切な診査診断のもと、個々の症例に応じた治療方針を立てることが望まれます。
また、PDF-FD療法を検討する際には、適応だけでなく実際の治療の流れや期間、費用について理解しておくことも大切です。
次章では、治療プロセスと現実的な負担について詳しく解説します。
PDF-FD療法の治療の流れ・期間・費用
PDF-FD療法を検討する際には、治療の具体的な流れや必要な期間、費用の目安を理解しておくことが重要です。歯周病治療は段階的に進められることが多く、PDF-FD療法はあくまで包括的治療計画の中で位置づけられます。
また、症例の状態や医療機関の方針によってプロセスが異なる場合があるため、詳細は事前のカウンセリングで確認することが望ましいでしょう。
1)治療の基本的な流れ
①初診・精密検査
まずは歯周ポケットの測定、X線撮影、必要に応じてCT検査などを行い、歯槽骨の状態や骨欠損の形態を評価します。これにより、再生療法の適応があるかどうかを判断します。
②基本治療(歯周基本治療)
スケーリングやルートプレーニングによって歯石や細菌性バイオフィルムを除去し、炎症のコントロールを図ります。この段階が不十分な場合、PDF-FD療法の効果が得られにくくなる可能性があります。
③採血とPDF-FD製剤の準備

PDF-FD療法が適応となる場合は、患者自身の血液を採取します。
④PDF-FD製剤の作製
採血した血液は専用のラボで血漿由来成長因子を抽出したうえで凍結乾燥処理を行い、製剤化します。採血後約2週間で完成します。
⑤歯周外科治療との併用
骨欠損が認められる場合にはフラップ手術などの歯周外科処置が行われることがあります。感染組織を除去した後、欠損部へPDF-FD製剤を適用し、修復環境の改善を目指します。
⑥術後管理とメンテナンス
治療後は定期的な経過観察とプロフェッショナルケアが重要です。適切なメンテナンスが行われない場合、どんな治療法を施しても歯周病が再発する可能性があります。
2)治療期間の目安
PDF-FD療法を含む歯周治療は、短期間で完結するものではありません。
骨の再構築には時間を要するため、最終的な評価は半年〜1年ほどかけて行われることもあります。
3)投与回数の考え方
歯科医師の判断で、必要に応じて複数回のPDF-FD治療を行います。
PDF-FD療法は「回数を重ねれば必ず効果が高まる」という性質の治療ではありません。
医師の観察・管理の下に、症状に応じて回数が検討されます。
4)費用の目安と保険適用
PDF-FD療法は自由診療であり、費用は医療機関や治療範囲によって差があります。
相場としては、1部位1回あたり7万円〜10万円程度が一つの目安とされています。
なお、歯周外科治療や骨補填材を併用する場合には追加費用が発生することがあります。総額は治療計画によって大きく変動するため、事前に見積もりを確認することが重要です。
歯周病の治療において、費用は重要な判断材料の一つですが、それだけで治療を選択することは望ましくありません。重要なのは、自分に適した治療法であるかどうか、そして長期的に歯の保存につながる可能性があるかという視点です。
治療内容や期待できる効果、リスクについて、歯科医師から十分な説明を受け、納得したうえで選択することが大切です。
PDF-FD療法の安全性とリスク・受ける際の注意点

PDF-FD療法は自己血由来の成長因子を活用する治療であり、生体適合性の観点から安全性に配慮されたアプローチと考えられています。しかし、すべての医療行為と同様に一定のリスクが存在するため、期待できる効果だけでなく副作用や限界についても理解しておくことが重要です。
また、治療後の経過は患者の全身状態や歯周病の進行度、術後のメンテナンス状況など多くの要因に左右される可能性があります。適切な診査診断のもとで治療を受けることが、安全性を高めるうえで不可欠です。
1)自己血由来製剤の特徴と安全性
PDF-FD療法は患者自身の血液を原料とするため、異物反応や免疫拒絶が起こるリスクは理論的に低いとされています。
さらに細胞を含まないCell Free製剤であることから、細胞移植に伴う生着不全などのリスクを考慮する必要がない点も特徴です。
ただし、自己血由来であっても完全にリスクがゼロになるわけではありません。採血や外科処置を伴う以上、他の治療と同じく医療リスクは存在します。
2)術後に起こり得る主な副作用
PDF-FD療法を含む歯周外科治療では、次のような一時的症状がみられることがあります。
- 腫脹(腫れ)
- 軽度の疼痛
- 出血
- 違和感
- 内出血
多くは創傷治癒の過程で生じる反応であり、通常は数日〜1週間程度で改善するとされています。ただし、症状が長引く場合には医療機関への相談が必要です。
3)感染リスクと無菌管理の重要性
歯周外科処置を伴う治療では、感染予防が極めて重要です。使用する器具の滅菌管理や適切な術野の確保など、医療機関の衛生管理体制が治療の安全性に直結します。
そのため、治療を受ける際には設備だけでなく、感染対策への取り組みについても確認することが望ましいでしょう。
4)全身状態が治癒に与える影響
創傷治癒は局所環境だけでなく、全身状態の影響も受けます。
- 喫煙
血流低下を引き起こし、組織修復を遅らせる可能性があります。
- 糖尿病
血糖コントロールが不良な場合、感染リスクや治癒遅延の要因となることがあります。
- 免疫機能の低下
術後回復に影響を及ぼす可能性があります。
これらの因子がある場合には、治療前に十分な評価を行うことが重要です。
5)医療機関選びが安全性を左右する
PDF-FD療法の適応は、適切な診断能力と外科的技術が求められます。安全性を高めるためには、次のような視点で医療機関を選ぶことが重要です。
- 歯周治療の実績が豊富
- 精密検査を実施しているか
- 治療計画の説明が十分か
- リスクについても説明しているか
- 術後フォロー体制が整っているか
6)術後管理とメンテナンスの重要性
歯周病は慢性疾患であり、治療後も継続的な管理が不可欠です。適切なセルフケアと定期的なプロフェッショナルケアを行うことで、再発リスクの低減につながります。
再生療法は「治療すれば終わり」ではなく、長期的な口腔管理の一部として捉えることが重要です。
7)治療効果の個人差と限界
PDF-FD療法は歯周組織の修復環境を整えることを目的とした補助療法であり、すべての症例で同様の結果が得られるわけではありません。骨欠損の形態や炎症の程度、生活習慣などによって治療結果は左右される可能性があります。
また、失われた組織を完全に元の状態へ戻す治療ではない点も理解しておく必要があります。過度な期待を抱くのではなく、現実的な治療目標を共有することが重要です。
歯周病やPDF-FD療法に関するよくある質問(FAQ)

PDF-FD療法について理解を深める中で、「本当に歯周病は改善するのか」「どの治療を選ぶべきか」といった疑問を持つ方も多いでしょう。
ここでは、患者さんからよく寄せられる質問に専門的視点からお答えします。
Q1.歯周病は完全に治りますか?
歯周病は慢性的に進行する疾患であり、一度失われた歯槽骨や歯周組織が完全に元の状態へ戻るとは限りません。しかし、適切な基本治療と継続的なメンテナンスによって炎症をコントロールし、進行を抑えることは可能とされています。PDF-FD療法は組織修復が進みやすい環境を整える補助的治療として用いられることがありますが、単独で歯周病を完治させるものではありません。長期的な口腔管理が重要です。
Q2.従来治療とどちらを選ぶべきですか?
歯周病治療の基本は、スケーリングやルートプレーニングなどによる原因除去です。再生療法はこれらの基本治療が適切に行われたうえで検討される補助的アプローチとされています。骨欠損の形態や歯の保存可能性によって適した治療は異なるため、どちらが優れているかを一概に判断することはできません。歯科医師による精密な診査診断を受け、自身の症例に適した治療方針を選択することが重要です。
Q3.効果を実感するまでどのくらいかかりますか?
歯周組織の修復には一定の時間を要します。術後の初期治癒は数週間程度で進みますが、組織が安定するまでには一般的に3〜6か月ほどかかるとされています。骨の再構築を含めた最終的な評価は、半年から1年程度の経過観察を経て行われることもあります。治癒速度は年齢や全身状態、生活習慣などによっても左右されるため、焦らず長期的な視点で治療に取り組むことが大切です。
Q4.PDF-FD療法に痛みやダウンタイムはありますか?
PDF-FD製剤の注入時の痛み術後に軽度の痛みや腫れ、違和感が生じることがありますが、多くは数日から1週間以内で改善するとされています。必要に応じて鎮痛薬が処方されることもあります。ダウンタイムの程度は治療範囲や個人差によって異なりますが、強い症状が長期間続く場合は早めに医療機関へ相談することが重要です。
Q5.他の歯周病治療と併用できますか?
PDF-FD療法は単独で行われることもありますが、多くの場合は歯周外科治療や骨補填材、GTR法などと組み合わせて使用されます。これにより骨の足場となる構造と生物学的修復環境の両方を整えることが期待されます。ただし、すべての症例に併用が適しているわけではないため、治療計画は個々の状態に応じて慎重に検討されます。
Q6.PDF-FD療法は誰でも受けられますか?
いいえ、下記の場合は禁忌(施術を受けられない)です。
- 活動性の感染
- 血液疾患・血小板異常
- 活動性がん
- 治療部位の感染や炎症
また、次のケースも慎重な判断が必要です。
- 重度の歯周病
- 自己免疫疾患
- 妊娠・授乳中
- 抗凝固薬・NSAIDs・ステロイド使用
- 過度の喫煙・飲酒
- 未コントロールの糖尿病・重度貧血・慢性疾患
- 最近のステロイド注射や大手術後
歯科医師による診査を受け、適応の有無を確認しましょう。
まとめ:歯周病治療におけるPDF-FD療法の位置づけ
本記事では、歯周病に対するPDF-FD療法の効果と安全性について、現在得られている医学的知見をもとに整理しました。
PDF-FD療法は、血漿由来の成長因子を活用して歯周組織の修復環境を整えることを目的とした治療アプローチです。近年、PRP療法をはじめとする歯周組織再生療法に関する研究が蓄積されており、適切な症例においては補助的治療として一定の臨床的有用性が示唆されています。
ただし、現時点では歯周病治療の標準治療として確立されているわけではなく、基本治療を代替するものではありません。
また、治療効果は骨欠損の形態や炎症の程度、全身状態、術後管理など多くの要因に影響される可能性があります。
歯周病は慢性的に進行する疾患であり、長期的な管理が予後を左右します。
改善の効果は、PDF-FD療法に限らず歯科での治療で完結するわけではなく、継続的な適切なプラークコントロールと定期的なメンテナンスを継続することが不可欠です。
今後はPDF-FD製剤の品質管理や投与方法の標準化、長期予後を評価する臨床研究の蓄積が期待されます。治療技術は進歩を続けていますが、重要なのは個々の症例に適した治療を選択することです。歯科医師による十分な説明を受け、効果と限界の双方を理解したうえで判断することが望ましいでしょう。
1)現時点での評価
PDF-FD療法は成長因子を利用した再生誘導型アプローチとして注目されています。血小板由来製剤に関する研究では、歯周ポケット深さの減少や臨床的アタッチメントレベルの獲得など、組織修復を支持する効果が期待されます、
一方で、PDF-FDに特化した大規模臨床試験はまだなく、今後はエビデンスの蓄積が求められています。そのため、現段階では「有望な補助療法」と位置づけるのが適切といえるでしょう。
2)補助的治療としての可能性
PDF-FD療法は単独で歯周組織を再生させる治療ではなく、生体が本来持つ創傷治癒能力を支援することを目的としています。特に、垂直性骨欠損など適応を慎重に選択した症例では、外科治療と併用することで修復環境の向上が期待されます。
重要なのは、「万能な治療」ではないという理解です。包括的な歯周治療の一要素として活用されることで、その価値が発揮されると考えられます。
3)基本治療とメンテナンスの重要性
歯周病治療の根幹は、原因となる細菌性プラークの管理にあります。どれほど先進的な治療を行ったとしても、口腔衛生状態が維持されなければ再発リスクは高まります。
そのため、スケーリングやルートプレーニングといった基本治療を徹底し、治療後も定期的なメンテナンスを継続することが長期的な歯の保存につながります。再生療法はあくまでその基盤の上に成り立つ治療であることを理解しておくことが重要です。
4)今後の研究と臨床応用への期待
再生治療や再生誘導型治療の分野は現在も進化を続けています。今後はPDF-FD療法に関する無作為化比較試験(RCT)や長期追跡研究が進むことで、より明確な適応基準や治療プロトコルが確立されていく可能性があります。
歯周病治療においては、「歯を保存する」という視点がますます重要視されています。新しい治療技術の可能性を正しく理解しつつ、科学的根拠に基づいた治療選択を行うことが、将来的な口腔健康の維持につながるでしょう。
<参照論文>
PMID: 35886083|PMCID: PMC9317493|DOI: 10.3390/ijerph19148232
日本語要旨:日本の口腔保健の現状を概観し、歯周病が歯の喪失に関与する背景や高齢化との関係を整理されている。日本で歯を失う主要因のエビデンス。
PMID: 29926951|DOI: 10.1002/JPER.17-0721
日本語要旨:歯周炎を単なる歯肉炎と区別し、歯周組織(歯槽骨・歯根膜など)の破壊を伴う慢性疾患として整理されている。歯周病の不可逆性の医学的根拠。
PMID: 23631572|DOI: 10.1902/jop.2013.1340011
日本語要旨:歯周病と糖尿病の双方向性(血糖と歯周炎症が相互に悪化)を整理したコンセンサス。全身疾患との関連(糖尿病)の根拠。
PMID: 25261053|PMCID: PMC4293771|DOI: 10.1177/0022034514552491
日本語要旨:重度歯周炎の世界的負担を推計した系統的レビュー。歯周病が高頻度で公衆衛生上重要である点を裏づけでき、放置で重大化することの根拠。
PMID: 39468505|PMCID: PMC11520879|DOI: 10.1186/s12903-024-04907-1
日本語要旨:歯周病と心血管疾患の関連を、複数のSR/メタ解析を束ねて評価。関連は支持されるが交絡や因果は慎重に解釈と整理できる。
PMID: 30585445|PMCID: PMC6431686|DOI: 10.1002/sctm.18-0181
日本語要旨:幹細胞を用いた歯周組織再生の戦略と臨床応用の可能性を概説。骨・歯根膜・セメント質の再建を目指す再生医療の将来性を示し、新規再生アプローチの理解に役立つ。
PMID: 15655028|DOI: 10.1111/j.1600-0757.2004.37101.x
日本語要旨:GTR(歯周組織誘導法)のintrabony defectに対する有効性を体系的に評価したCochraneレビュー。臨床的付着の獲得やポケット深さの改善が報告され、歯周組織再生療法の代表的術式としての根拠を示す重要文献。
PMID: 20467602
日本語要旨:エムドゲイン(エナメルマトリックスタンパク)のintrabony defectに対する効果をCochraneで検証。CALやPDの改善が示される一方、研究の異質性が指摘され、症例選択の重要性を示唆する。
PMID: 26547659 DOI: 10.1002/jbmr.2738
日本語要旨:rhFGF-2(トラフェルミン:日本ではリグロスの有効成分)をintrabony defectで検証した第III相比較試験。骨増生などでEMDに対する非劣性/優越が示され、安全性も評価されている。
PMID: 28419559|DOI: 10.1111/jcpe.12732
日本語要旨:歯周病の世界的負担と健康への影響を整理し、機能・栄養・生活の質に及ぼす重要性を強調。歯周疾患を全身的健康課題として捉える根拠となる総説。
PMID: 32962283|PMCID: PMC7555364|DOI: 10.3390/ijms21186904
日本語要旨:PRPの凍結乾燥(FD-PRP)により、サイトカイン/成長因子の機能保持と保存性向上、標準化(再現性)を目指す考え方を総説として整理。PDF-FDの「安定性・均一性」説明の根拠。。
PMID: 33919726|PMCID: PMC8070716|DOI: 10.3390/jcm10081678
日本語要旨:自己血由来FD-PRPを凍結乾燥・保存後に骨造成へ応用し、安全性(有害事象の有無等)を中心に検討したパイロット研究。PDF-FD療法の「医療行為としての管理・安全性」の説明の根拠。。
PMID: 28670400|PMCID: PMC5481587|DOI: 10.4184/asj.2017.11.3.329
日本語要旨:PRPを凍結乾燥して保存した場合、室温保存より成長因子発現の保持が良好で、長期保存でも生物活性が維持され得ることを示した基礎研究。凍結乾燥で活性保持の根拠。
PMID: 31575111|PMCID: PMC7010512|DOI: 10.31616/asj.2019.0048
日本語要旨:FD-PRPを一定期間保存後でも、PDGF受容体〜ERK経路の活性化や細胞増殖誘導が確認され、成長因子の薬理活性が保持される可能性を示した。「活性維持・再現性」の説明の根拠。
PMID: 30284954|DOI: 10.2217/rme-2018-0035
日本語要旨:新鮮PRPと凍結乾燥PRPを比較し、主要成長因子レベルや細胞増殖誘導など機能面が維持され得ることを示した比較研究。PRPとの差(保存性・品質)説明の根拠。
PMID: 37435111|DOI: 10.1155/2023/1099013
日本語要旨:血小板由来製剤(PRF/PRP等)の歯周組織再生効果を俯瞰。ポケット減少・CAL獲得・骨充填の改善を示す報告が多い一方、症例選択と研究品質が鍵。
PMID: 33609186|DOI: 10.1007/s00784-021-03825-8
日本語要旨:歯周骨内欠損に対するPRFの有効性を統合評価。外科単独よりPD減少・CAL獲得・骨充填が改善する傾向。PDF-FD同様の成長因子補助の根拠。
PMID: 38771493|DOI: 10.1007/s10266-024-00949-7
日本語要旨:PRFを用いた骨内欠損治療をネットワークメタ解析で比較。CAL/PD/骨充填の指標で相対効果を整理し、血小板由来因子(PDF-FD含む)活用の位置づけの説明。
PMID: 27531202|DOI: 10.1186/s12903-016-0261-5
日本語要旨:骨内欠損の外科治療にPRPを追加した効果を統合。CAL獲得・PD減少の上乗せが示唆される一方、GTR併用条件などで差が出る点を整理し、適応選定の重要性を示す。
PMID: 22348695|DOI: 10.1902/jop.2012.110705
日本語要旨:3壁性骨内欠損でPRFとPRPをRCT比較。PD減少・CAL獲得・骨充填で両者が改善し、差は限定的。PDF-FD(成長因子主体)でも「補助療法」位置づけの根拠。
PMID: 16996004|DOI: —
日本語要旨:ヒト骨内欠損でPRP併用の臨床効果を検証。骨補填材併用群でPD・CAL・画像上の骨増加が良好と報告。PDF-FDの「局所修復環境づくり」の考え方を補助。
SNS Share
\ この記事をシェアする /
